-
摘要: 由于微流控芯片具有优异的集成性和灵活的可操作性,基于芯片上的检测方法被大量开发,发展十分迅速。其中,表面增强拉曼光谱(SERS)凭借其超高的灵敏度、独一无二的指纹谱和窄峰宽等特点成为一种广泛采用的检测手段。SERS微流控芯片集SERS检测技术与微流控芯片的优势于一体,一方面为SERS检测方法的重复性和可靠性提供了一个高效平台,另一方面推动了微流控芯片的功能拓展,在生物分子探测、细胞捕获乃至组织模拟等领域具有广阔的应用前景。本文在简要介绍SERS的原理及其生物传感应用的基础上,重点概述了SERS微流控芯片的构建及其在生物传感及检测中的应用,最后探讨了该研究方向存在的问题及发展方向。Abstract: With excellent integrability and flexible operability, microfluidic chips have been developed rapidly. Among them, Surface-enhanced Raman Spectroscopy (SERS) has become a widely used detection technique due to its ultrasensitivity, unique fingerprint spectrum and narrow spectroscopic bands. The SERS microfluidic chip integrates the advantages of the SERS detection technology and the microfluidic chip. On the one hand, it provides an efficient platform for the repeatability and reliability of the SERS detection method. On the other hand, it promotes function expansion for microfluidic chips. The SERS microfluidic chips have broad application prospects in the fields of biomolecule detection, cell capture and even tissue simulation. In this review, the principle of SERS is briefly introduced, and the construction of SERS microfluidic chip and its applications in biosensing and detection are emphatically summarized. Finally, the problems and development direction of the research are proposed.
-
Key words:
- surface-enhanced raman spectroscopy /
- microfluidic /
- SERS microfluidic chip /
- biosensing
-
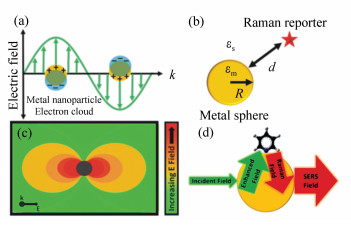
图 1 (a) 电子云振荡的图示,对于小于光波长的纳米粒子而言其电子云振荡方向与电场矢量方向相反; (b)描绘正文中公式1的参数; (c)在光激发下金属纳米粒子发射的偶极子场; (d)入射场和出射场的电磁增强
Figure 1. (a)Illustration of the oscillating electron cloud, which moves in opposite direction of the electric field vector, for a nanoparticle smaller than the wavelength of light; (b)depiction of the parameters used in eq 1 of the main text; (c)emitted dipole field of a metallic nanoparticle under light excitation; (d)EE of both the incident field and the scattered field
图 3 (a) L形纳米三聚体的TEM图,在二氧化硅壳内包裹三个修饰PCEPE的金核;(b)3D自组装等离子体超结构的TEM图,在硅壳内包裹80纳米金核和众多单分散的20纳米金纳米卫星粒子
Figure 3. (a)TEM image of an L-shaped trimer nanoantenna comprised of three Au cores functionalized with PCEPE (structure shown) and encapsulated in a SiO2 shell; (b)TEM images of 3D self-assembled plasmonic superstructure comprising a silica-encapsulated 80 nm Au core and multiple monodisperse 20 nm Au satellite particles
图 4 (a) BT修饰的Ag-PAO模板的SEM图,由氧化铝基质在0.1 M氢氧化钠溶液中部分分解得到;(b)52°倾角的带有6纳米IPS和150 nm硅纳米柱的NOSP二聚体SEM图;(c)非接触模式TERS;(d)SHINER:壳分离模式;(e)用纳米球印刷术制成的规则SERS基底方法示意图
Figure 4. (a)SEM image of BT-modified Ag-PAO templates obtained by partial dissolution of the alumina matrix in 0.1 M aqueous NaOH; (b)SEM image at a 52° tilted view of the NOSP dimers with a 6-nm IPS and 150-nm Si pillar height; (c)Tip-enhanced Raman spectroscopy: noncontact mode; (d)SHINERS: shell-isolated mode; (e)schematic diagram of template methods using nanosphere lithography to fabricate ordered nanostructured SERS-active substrates
图 5 (a) 基于金纳米粒子-金纳米棒复合体检测BPA的SERS适体探针示意图;(b)检测ATP的SERS比率计硅片适体探针示意图;(c)银@介孔硅@银三层核壳结构纳米粒子制备流程示意图;(d)合成19种SERS编码纳米粒子的编码、结构及光谱
Figure 5. (a)Scheme of SERS aptasensor for the detection of BPA based on gold nanoparticle-nanorod heteroassembly; (b)Schematic illustration of the ratiometric silicon SERS aptasensor for ATP detection; (c)proposed preparation process of Ag@MSiO2@Ag TCSNPs; (d)codes, structures and measured spectra of the synthesized 19 SERS encoders
图 6 (a) A:实验结构示意图。B:基于SERS的侧向流条带实验定量检测HIV-1 DNA的检测原理。(C为对照组,T为实验组);(b)银纳米金字塔由DNA框架自组装SERS分析生物标志物示意图。C:通过外泌体、磁球和SERS探针间免疫识别形成的三明治结构;(c)利用BODIPY修饰的纳米粒子SERS成像示意图;(d)SERS探针与基因组DNA的杂交原理示意图
Figure 6. (a)A:Schematic illustration of the configuration. B:The measurement principle of the SERS-based lateral flow assay for quantification of HIV-1 DNA.(C is the control line and T is the test line); (b)Scheme of Ag pyramids self-assembled by DNA frame for SERS analysis of biomarkers; (c)schematic representation of the targeted SERS imaging using aza-BODIPY attached to NPs; (d)schematic Illustration of the Hybridization between the SERS Nanoprobes and Genome DNA
图 7 (a) A:硅壳金纳米粒子探针的SERS光谱(左)及拉曼分子的分子结构(右)。B:使用不同拉曼分子的SERS标签典型的拉曼光谱(左)及相应的编码(右)。(b)合成的15种纳米粒子的构成、光谱和编码
Figure 7. (a)A:SERS spectra of AuNPs-Ra@SiO2(left) and molecular structures of Raman reporters employed in this study(right). B:Typical Raman spectra(left) on microbeads with different types of SERS label using different Raman reporter (10000, 01000, 00100, 00010, 00001 and 11111) and their corresponding spectral barcodes(right). (b)Composition, measured spectra, and codes of the synthesized 15 nanoparticles
图 8 (a) 集成DNA竞争取代序列检测的SERRS微流微系统。修饰DNA探针-报告分子对的二氧化硅微球(插图)充满一个区块。当目标序列引入到入口时,拉曼分子的链被取代。它们沿着通道流动时与金属纳米聚集体混合并被捕获在微流芯片中的SERRS检测区域。(b)A:基于SERS竞争吸附免疫检测的螺旋线双通道微流传感器示意图。传感器由两个平行的通道组成:一个检测PGA(浅灰),另一个作对照(深灰)。B:注满四种不同颜色墨水的芯片图像。C:磁性免疫检测的捕获区域图。(c)用带气阀的通道捕获与释放金纳米粒子进行SERS检测的示意图。(d)光电微流SERS光谱。小量样品的光电微流设备集成到一个传统的SERS检测系统。用一个激光光源可以同时达到使金属纳米粒子聚集和SERS信号的检测的目的
Figure 8. (a)Microfluidic SERRS microsystem with integrated competitive displacement for DNA sequence detection. Silica microspheres functionalized with DNA probe-reporter pairs(inset) are packed against a frit. When the target sequence is introduced at the inlet, Raman-labeled reporter oligos are displaced. As they flow along the channel, they are mixed with metal nanoclusters and trapped in the microfluidic SERRS detection region. (b)A:Schematic illustration of the solenoid-embedded dual channel microfluidic sensor for SERS-based competitive immunoassay. The sensor is composed of two parallel channels: one for PGA sensing(light gray) and the other for control(dark gray). B:optical images of the solenoid chip filled with four different colors of inks. C:photograph of the capture area for magnetic immunocomplexes. (c)Schematics of trapping and releasing of gold nanoparticles using a modified pneumatic microvalve for SERS detection. (d)Experimental setup for optoelectrofluidic SERS spectroscopy. An optoelectrofluidic device containing a tiny volume of sample droplet is integrated into a conventional SERS detection system. Both concentration of metal nanoparticles for SERS enhancement and detection of SERS signal are simultaneously achieved with a single laser source
图 10 (a) 在微流芯片内激光制造SMA的示意图;(b)A:微流芯片内三个模块示意图,分别用红、绿和蓝色方块表示注射、混合和光学检测功能区。B:光引导银纳米聚集体的形成过程及原位SERS检测。注射区的硝酸银、水、CV和柠檬酸钠溶液用不同颜色表示。微流通道内的流动用白色箭头指示
Figure 10. (a)Scheme for laser fabrication of SMAs inside a microfluidic channel; (b)A:schematic of microfluidic chip with three modules functioning as injection, mixing, and optical detection marked by the red, green, and blue squares, respectively. B:the procedure of photoinduced growth of silver nanoaggregates and in situ SERS measurements. The solutions of AgNO3, H2O, CV and sodium citrate in the injection module are represented by different colors. The flow in the microchannel is indicated by the white arrows
图 11 (a) 在硅片上修饰银纳米粒子作为基底集成在微流芯片上,A:一步法,B:两步法检测miRNA;(b)基于SERS的液滴微流传感器免清洗的磁性免疫检测示意图。这种传感器由5个部分组成,功能如下:ⅰ液滴生成及试剂混合;ⅱ形成磁性免疫复合物;ⅲ磁铁分离免疫复合物;ⅳ含有上清的更大的液滴生成来进行SERS检测;ⅴ含有磁性免疫复合物的更小的液滴生成;(c)微流芯片构成及概念示意图。细胞预先标记肿瘤特异性与对照探针(后者两种细胞都有修饰),再注入芯片中,流向中心汇集后通过拉曼激光照射;(d)微流芯片示意图:A:顶视图B:侧视图。这一设备有两层:液体流动层(黑线)和调节流动层连接的控制层(粉色和蓝色图案)。在侧视图中芯片由3个功能区域组成。区域Ⅰ:细胞培养池(癌细胞);区域Ⅱ:抗体条码(不同通道内基底与抗体相匹配);区域Ⅲ:细胞培养池(免疫细胞被基底上的抗体捕获)
Figure 11. (a)Microfluidic chip integrating pSi membranes decorated by Ag NPs and detection schemes of miRNA by A:one-step hybridization assay, B:two-step hybridization assay; (b)schematic illustration of the SERS-based microdroplet sensor for wash-free magnetic immunoassay. The sensor is composed of five compartments with the following functions: (ⅰ)droplet generation and reagent mixing, (ⅱ)formation of magnetic immunocomplexes, (ⅲ)magnetic bar-mediated isolation of immunocomplexes, (ⅳ)generation of larger droplets containing the supernatant for SERS detection and (ⅴ)generation of smaller droplets containing magnetic immunocomplexes; (c)schematic of setup and concept. Cells, prelabeled with a cocktail of cancer-specific(NRP) and control(UC) SBTs (the latter binding both cell types), are injected into the device, where they are flow-focused before passing through the Raman laser; (d)schematic illustration of a microfluidic chip: A: top view and B: side view. The device contains two layers: a flow layer (black line) for transport of fluids and a control layer(pink and blue pattern) to regulate the connections in the flow layer. In the side view, the chip is composed of three functional sections. Section Ⅰ the cell culture chamber (cancer cells); section Ⅱ:antibody barcode(the substrate is patterned with various antibodies in different channels); section Ⅲ:the cell culture chamber(immune cells are captured by the antibody on the substrate)
图 12 (a) A:用来检测砷离子的微流芯片示意图。砷离子与GSH/4-MPY修饰的纳米粒子在之字形微流通道内快速、充分混合(插图)。B:砷离子的分析原理。当砷离子与GSH/4-MPY修饰的纳米粒子耦合时发生聚集,银纳米粒子上的4-MPY的拉曼信号被增强;(b)A:液滴微流设备的示意图。B:银壳金纳米棒的SERS光谱(红色)及加入硫氰酸离子后的SERS光谱(蓝色)
Figure 12. (a)A:schematic diagram of the microfluidic chip used for analyzing the As(Ⅲ) ions. The rapid, full mixing of the As(Ⅲ) ions and GSH/4-MPY functionalized AgNPs achieved in a zigzag(75 angles) microfluidic channel(inset). B:the analytical principle for As(Ⅲ) ions. When As(Ⅲ) ions couple with GSH/4-MPY functionalized AgNPs, aggregation occurs and the Raman signals are improved when 4-MPY is adsorbed on the surface of the AgNPs; (b)A:schematic illustration of the droplet microfluidic device. B:SERS spectra of CTAB-stabilized Au@Ag NRs(red curve) and Au@Ag NRs with the addition of SCN-(blue curve)
图 13 (a) A:光流控SERS微系统示意图。B:光流控SERS系统。C:充满的微球和集成的光纤;(b)牛奶中三聚氰胺检测的比较使用A:标准的FDA过程和B:我们的纳米柱检测方案。在显示金纳米柱芯片用于分子检测同时展示的具有代表性的SEM图为打开(左)和关闭(右)的金纳米柱五聚物分别对应处理过滤的牛奶前后
Figure 13. (a)A:schematic of optofluidic SERS microsystem. B:photo of optofluidic SERS microsystem. C:micrograph of packed microspheres and integrated fiber optic cables; (b)Comparison of melamine sensing in milk using A:a standard FDA procedure versus B: our nanofinger-based sensing solution. The representative SEM images of open(left) and closed(right) pentamer gold nanofingers before and after treatment with the filtered milk, respectively, are shown along with the illustration of how the gold nanofinger chips were used for molecular sensing
-
[1] VAN DEN BERG A, BERGVELD P. Labs-on-a-chip:origin, highlights and future perspectives. On the occasion of the 10th microtas conference[J]. Lab. Chip, 2006, 6(10):1266-1273. doi: 10.1039/B612120A [2] HUANG J A, ZHANG Y L, DING H, et al.. SERS-enabled lab-on-a-chip systems[J]. Advanced Optical Materials, 2015, 3(5):618-633. doi: 10.1002/adom.v3.5 [3] CARRASCOSA L G, HUERTAS C S, LECHUGA L M. Prospects of optical biosensors for emerging label-free RNA analysis[J]. Trac-Trends in Analytical Chemistry, 2016, 80:177-189. doi: 10.1016/j.trac.2016.02.018 [4] AVELLA-OLIVER M, PUCHADES R, WACHSMANN-HOGIU S, et al.. Label-free SERS analysis of proteins and exosomes with large-scale substrates from recordable compact disks[J]. Sensors and Actuators B-Chemical, 2017, 252:657-662. doi: 10.1016/j.snb.2017.06.058 [5] ZRIMSEK A B, CHIANG N H, MATTEI M, et al.. Single-molecule chemistry with surface-and tip-enhanced Raman spectroscopy[J]. Chemical Reviews, 2017, 117(11):7583-7613. doi: 10.1021/acs.chemrev.6b00552 [6] WU L, WANG Z, ZONG S, et al.. Simultaneous evaluation of p53 and p21 expression level for early cancer diagnosis using SERS technique[J]. Analyst, 2013, 138(12):3450-3456. doi: 10.1039/c3an00181d [7] NGUYEN A H, LEE J, CHOI H I, et al.. Fabrication of plasmon length-based surface enhanced Raman scattering for multiplex detection on microfluidic device[J]. Biosensors & Bioelectronics, 2015, 70:358-365. http://cn.bing.com/academic/profile?id=20666eca2c4ef5bed980f8d3b3d6afb8&encoded=0&v=paper_preview&mkt=zh-cn [8] JAHN I J, ZUKOVSKAJA O, ZHENG X S, et al.. Surface-enhanced Raman spectroscopy and microfluidic platforms:challenges, solutions and potential applications[J]. Analyst, 2017, 142(7):1022-1047. doi: 10.1039/C7AN00118E [9] ZHOU Q, KIM T. Review of microfluidic approaches for surface-enhanced Raman scattering[J]. Sensors and Actuators B-Chemical, 2016, 227:504-514. doi: 10.1016/j.snb.2015.12.069 [10] RAMAN C V, KRISHNAN K S. A new type of secondary radiation(reprinted from nature, vol 121, pp 501-502, 1928)[J]. Current Science, 1998, 74(4):381-381. http://cn.bing.com/academic/profile?id=ea37b5c9e8356c64d15f14096400404d&encoded=0&v=paper_preview&mkt=zh-cn [11] FLEISCHMANN M, HENDRA P J, MCQUILLAN A J. Raman-spectra of pyridine adsorbed at a silver electrode[J]. Chemical Physics Letters, 1974, 26(2):163-166. doi: 10.1016/0009-2614(74)85388-1 [12] SCHLUCKER S. Surface-enhanced Raman spectroscopy:concepts and chemical applications[J]. Angewandte Chemie International Edition, 2014, 53(19):4756-4795. doi: 10.1002/anie.201205748 [13] LE RU E C, MEYER S A, ARTUR C, et al.. Experimental demonstration of surface selection rules for SERS on flat metallic surfaces[J]. Chemical Communications(Camb), 2011, 47(13):3903-3905. http://cn.bing.com/academic/profile?id=50d04142b1d818f307452257b8e6dd7d&encoded=0&v=paper_preview&mkt=zh-cn [14] HARMSEN S, HUANG R M, WALL M A, et al.. Surface-enhanced resonance Raman scattering nanostars for high-precision cancer imaging[J]. Science Translational Medicine, 2015, 7(271):11. http://cn.bing.com/academic/profile?id=f7ab25e34e7177676cffa8dc9a83c04b&encoded=0&v=paper_preview&mkt=zh-cn [15] ZHOU J J, XIONG Q R, MA J L, et al.. Polydopamine-enabled approach toward tailored plasmonic nanogapped nanoparticles:from nanogap engineering to multifunctionality[J]. ACS Nano, 2016, 10(12):11066-11075. doi: 10.1021/acsnano.6b05951 [16] DING S Y, YI J, LI J F, et al.. Nanostructure-based plasmon-enhanced Raman spectroscopy for surface analysis of materials[J]. Nature Reviews Materials, 2016, 1(6):16021. doi: 10.1038/natrevmats.2016.21 [17] ZONG S, WANG Z, CHEN H, et al.. Ultrasensitive telomerase activity detection by telomeric elongation controlled surface enhanced Raman scattering[J]. Small, 2013, 9(24):4215-4220. doi: 10.1002/smll.v9.24 [18] ZONG S, WANG Z, CHEN H, et al. Assessing telomere length using surface enhanced Raman scattering[J]. Scientific Reports, 2014, 4:6977. http://cn.bing.com/academic/profile?id=6f90e468d08888346fb5b161ead21cde&encoded=0&v=paper_preview&mkt=zh-cn [19] WANG Z, ZONG S, YANG J, et al. One-step functionalized gold nanorods as intracellular probe with improved SERS performance and reduced cytotoxicity[J]. Biosensors and Bioelectronics, 2010, 26(1):241-247. doi: 10.1016/j.bios.2010.06.032 [20] SENAPATI D, SINGH A K, RAY P C. Real time monitoring of the shape evolution of branched gold nanostructure[J]. Chemical Physics Letters, 2010, 487(1):88-91. http://cn.bing.com/academic/profile?id=faa6c15931e0aef46718e105aef8b30d&encoded=0&v=paper_preview&mkt=zh-cn [21] REGUERA J, LANGER J, DE ABERASTURI D J, et al.. Anisotropic metal nanoparticles for surface enhanced Raman scattering[J]. Chemical Society Reviews, 2017, 46(13):3866-3885. doi: 10.1039/C7CS00158D [22] PEI Y, WANG Z, ZONG S, et al.. Highly sensitive SERS-based immunoassay with simultaneous utilization of self-assembled substrates of gold nanostars and aggregates of gold nanostars[J]. Journal of Materials Chemistry B, 2013, 1(32):3992. doi: 10.1039/c3tb00519d [23] SONG C, WANG Z, ZHANG R, et al.. Highly sensitive immunoassay based on Raman reporter-labeled immuno-Au aggregates and SERS-active immune substrate[J]. Biosensors and Bioelectronics, 2009, 25(4):826-831. doi: 10.1016/j.bios.2009.08.035 [24] LIU M, WANG Z, ZONG S, et al.. SERS-based DNA detection in aqueous solutions using oligonucleotide-modified Ag nanoprisms and gold nanoparticles[J]. Analytical and Bioanalytical Chemistry, 2013, 405(18):6131-6136. doi: 10.1007/s00216-013-7016-9 [25] WUSTHOLZ K L, HENRY A-I, MCMAHON J M, et al.. Structure-activity relationships in gold nanoparticle dimers and trimers for surface-enhanced Raman spectroscopy[J]. Journal of the American Chemical Society, 2010, 132(31):10903-10910. doi: 10.1021/ja104174m [26] GELLNER M, STEINIGEWEG D, ICHILMANN S, et al.. 3d self-assembled plasmonic superstructures of gold nanospheres:synthesis and characterization at the single-particle level[J]. Small, 2011, 7(24):3445-3451. doi: 10.1002/smll.v7.24 [27] LEE S J, MORRILL A R, MOSKOVITS M. Hot spots in silver nanowire bundles for surface-enhanced Raman spectroscopy[J]. Journal of the American Chemical Society, 2006, 128(7):2200-2201. doi: 10.1021/ja0578350 [28] CHIRUMAMILLA M, TOMA A, GOPALAKRISHNAN A, et al.. 3d nanostar dimers with a sub-10-nm gap for single-/few-molecule surface-enhanced Raman scattering[J]. Advanced Materials, 2014, 26(15):2353-2358. doi: 10.1002/adma.v26.15 [29] LI J F, HUANG Y F, DING Y, et al.. Shell-isolated nanoparticle-enhanced Raman spectroscopy[J]. Nature, 2010, 464(7287):392-395. doi: 10.1038/nature08907 [30] WU D Y, LI J F, REN B, et al.. Electrochemical surface-enhanced Raman spectroscopy of nanostructures[J]. Chemical Society Reviews, 2008, 37(5):1025-1041. doi: 10.1039/b707872m [31] WANG Z, ZONG S, WU L, et al.. SERS-activated platforms for immunoassay:probes, encoding methods, and applications[J]. Chemical Reviews, 2017, 117(12):7910-7963. doi: 10.1021/acs.chemrev.7b00027 [32] FENG J, XU L, CUI G, et al.. Building SERS-active heteroassemblies for ultrasensitive bisphenol a detection[J]. Biosensors and Bioelectronics, 2016, 81:138-142. doi: 10.1016/j.bios.2016.02.055 [33] LI A, TANG L, SONG D, et al.. A SERS-active sensor based on heterogeneous gold nanostar core-silver nanoparticle satellite assemblies for ultrasensitive detection of aflatoxinb1[J]. Nanoscale, 2016, 8(4):1873-1878. doi: 10.1039/C5NR08372A [34] SHI H, CHEN N, SU Y, et al.. Reusable silicon-based surface-enhanced Raman scattering ratiometric aptasensor with high sensitivity, specificity, and reproducibility[J]. Analytical Chemistry, 2017, 89(19):10279-10285. doi: 10.1021/acs.analchem.7b01881 [35] JIANG T, WANG X, ZHOU J, et al. Hydrothermal synthesis of Ag@mSiO2@Ag three core-shell nanoparticles and their sensitive and stable SERS properties[J]. Nanoscale, 2016, 8(9):4908-4914. doi: 10.1039/C6NR00006A [36] FU X, CHENG Z, YU J, et al.. A SERS-based lateral flow assay biosensor for highly sensitive detection of HIV-1 DNA[J]. Biosensors and Bioelectronics, 2016, 78:530-537. doi: 10.1016/j.bios.2015.11.099 [37] XU L, YAN W, MA W, et al.. SERS encoded silver pyramids for attomolar detection of multiplexed disease biomarkers[J]. Advanced Materials, 2015, 27(10):1706-1711. doi: 10.1002/adma.201402244 [38] ADARSH N, RAMYA A N, MAITI K K, et al.. Unveiling nir Aza-boron-dipyrromethene(bodipy) dyes as raman probes:Surface-enhanced Raman scattering(SERS)-guided selective detection and imaging of human cancer cells[J]. Chemistry, 2017, 23(57):14286-14291. doi: 10.1002/chem.201702626 [39] ZONG S, CHEN C, WANG Z, et al. Surface enhanced Raman scattering based in situ hybridization strategy for telomere length assessment[J]. ACS Nano, 2016, 10(2):2950-2959. doi: 10.1021/acsnano.6b00198 [40] ZONG S, WANG Z, ZHANG R, et al. A multiplex and straightforward aqueous phase immunoassay protocol through the combination of SERS-fluorescence dual mode nanoprobes and magnetic nanobeads[J]. Biosensors and Bioelectronics, 2013, 41:745-751. doi: 10.1016/j.bios.2012.09.057 [41] LIU M, WANG Z, PAN L, et al.. A SERS/fluorescence dual-mode nanosensor based on the human telomeric g-quadruplex DNA:application to mercury(ii) detection[J]. Biosensors and Bioelectronics, 2015, 69:142-147. doi: 10.1016/j.bios.2015.02.009 [42] ZHANG Y, WANG Z, WU L, et al.. Rapid simultaneous detection of multi-pesticide residues on apple using sers technique[J]. Analyst, 2014, 139(20):5148-5154. doi: 10.1039/C4AN00771A [43] ZHU D, WANG Z, ZONG S, et al.. Wavenumber-intensity joint SERS encoding using silver nanoparticles for tumor cell targeting[J]. RSC Advances, 2014, 4(105):60936-60942. doi: 10.1039/C4RA11522H [44] LAI Y, SUN S, HE T, et al. Raman-encoded microbeads for spectral multiplexing with SERS detection[J]. RCS Advances, 2015, 5(18):13762-13767. [45] WANG Z, ZONG S, LI W, et al.. SERS-fluorescence joint spectral encoding using organic-metal-qd hybrid nanoparticles with a huge encoding capacity for high-throughput biodetection:putting theory into practice[J]. Journal of the American Chemical Society, 2012, 134(6):2993-3000. doi: 10.1021/ja208154m [46] HIDI I J, JAHN M, WEBER K, et al.. Lab-on-a-chip-surface enhanced Raman scattering combined with the standard addition method:toward the quantification of nitroxoline in spiked human urine samples[J]. Analytical Chemistry, 2016, 88(18):9173-9180. doi: 10.1021/acs.analchem.6b02316 [47] YAZDI S H, GILES K L, WHITE I M. Multiplexed detection of DNA sequences using a competitive displacement assay in a microfluidic SERRS-based device[J]. Analytical Chemistry, 2013, 85(21):10605-10611. doi: 10.1021/ac402744z [48] GAO R, KO J, CHA K, et al.. Fast and sensitive detection of an anthrax biomarker using SERS-based solenoid microfluidic sensor[J]. Biosensors and Bioelectronics, 2015, 72:230-236. doi: 10.1016/j.bios.2015.05.005 [49] ZHOU J, REN K, ZHAO Y, et al.. Convenient formation of nanoparticle aggregates on microfluidic chips for highly sensitive SERS detection of biomolecules[J]. Analytical and Bioanalytical Chemistry, 2012, 402(4):1601-1609. doi: 10.1007/s00216-011-5585-z [50] HWANG H, HAN D, OH Y J, et al.. In situ dynamic measurements of the enhanced SERS signal using an optoelectrofluidic sers platform[J]. Lab. Chip, 2011, 11(15):2518-2525. doi: 10.1039/c1lc20277d [51] OH Y J, JEONG K H. Optofluidic SERS chip with plasmonic nanoprobes self-aligned along microfluidic channels[J]. Lab. Chip, 2014, 14(5):865-868. doi: 10.1039/c3lc51257f [52] MAO H, WU W, SHE D, et al.. Microfluidic surface-enhanced Raman scattering sensors based on nanopillar forests realized by an oxygen-plasma-stripping-of-photoresist technique[J]. Small, 2014, 10(1):127-134. doi: 10.1002/smll.201300036 [53] XU B B, ZHANG R, LIU X Q, et al.. On-chip fabrication of silver microflower arrays as a catalytic microreactor for allowing in situ SERS monitoring[J]. Chemical Communications(Camb), 2012, 48(11):1680-1682. http://cn.bing.com/academic/profile?id=67551b96b57c845ba3b0d8218c2ce081&encoded=0&v=paper_preview&mkt=zh-cn [54] YAN W, YANG L, CHEN J, et al. In situ two-step photoreduced SERS materials for on-chip single-molecule spectroscopy with high reproducibility[J]. Advanced Materials, 2017, 29(36) http://cn.bing.com/academic/profile?id=6b3ab9c8aab2216f675e87fb2f7bf4b2&encoded=0&v=paper_preview&mkt=zh-cn [55] MUEHLIG A, BOCKLITZ T, LABUGGER I, et al.. Loc-sers:A promising closed system for the identification of mycobacteria[J]. Analytical Chemistry, 2016, 88(16):7998-8004. doi: 10.1021/acs.analchem.6b01152 [56] HIDI I J, JAHN M, PLETZ M W, et al.. Toward levofloxacin monitoring in human urine samples by employing the LoC-SERS technique[J]. Journal of Physical Chemistry C, 2016, 120(37):20613-20623. doi: 10.1021/acs.jpcc.6b01005 [57] ZOU K, GAO Z, DENG Q, et al.. Picomolar detection of carcinoembryonic antigen in whole blood using microfluidics and surface-enhanced Raman spectroscopy[J]. Electrophoresis, 2016, 37(5-6):786-789. doi: 10.1002/elps.v37.5-6 [58] NOVARA C, CHIADO A, PACCOTTI N, et al.. SERS-active metal-dielectric nanostructures integrated in microfluidic devices for label-free quantitative detection of miRNA[J]. Faraday Discuss, 2017, http://cn.bing.com/academic/profile?id=6bc20d9352b3600a5ccc153d945bc176&encoded=0&v=paper_preview&mkt=zh-cn [59] GAO R, CHENG Z, DEMELLO A J, et al.. Wash-free magnetic immunoassay of the psa cancer marker using SERS and droplet microfluidics[J]. Lab. Chip, 2016, 16(6):1022-1029. doi: 10.1039/C5LC01249J [60] PALLAORO A, HOONEJANI M R, BRAUN G B, et al.. Rapid identification by surface-enhanced Raman spectroscopy of cancer cells at low concentrations flowing in a microfluidic channel[J]. ACS Nano, 2015, 9(4):4328-4336. doi: 10.1021/acsnano.5b00750 [61] WU L, WANG Z, ZHANG Y, et al.. In situ probing of cell-cell communications with surface-enhanced Raman scattering(SERS) nanoprobes and microfluidic networks for screening of immunotherapeutic drugs[J]. Nano Research, 2016, 10(2):584-594. http://cn.bing.com/academic/profile?id=3d7d4e8fdc43201e7e1b444d52bbac4c&encoded=0&v=paper_preview&mkt=zh-cn [62] WU L, WANG Z, FAN K, et al.. A SERS-assisted 3d barcode chip for high-throughput biosensing[J]. Small, 2015, 11(23):2798-2806. doi: 10.1002/smll.201403474 [63] PATZE S, HUEBNER U, LIEBOLD F, et al.. SERS as an analytical tool in environmental science:the detection of sulfamethoxazole in the nanomolar range by applying a microfluidic cartridge setup[J]. Analytica Chimica Acta, 2017, 949:1-7. doi: 10.1016/j.aca.2016.10.009 [64] QI N, LI B, YOU H, et al.. Surface-enhanced Raman scattering on a zigzag microfluidic chip:towards high-sensitivity detection of As(Ⅲ) ions[J]. Analytical Methods, 2014, 6(12):4077-4082. doi: 10.1039/C3AY42283F [65] WU L, WANG Z, ZONG S, et al.. Rapid and reproducible analysis of thiocyanate in real human serum and saliva using a droplet SERS-microfluidic chip[J]. Biosensors and Bioelectronics, 2014, 62:13-18. doi: 10.1016/j.bios.2014.06.026 [66] CHOI J, LEE K S, JUNG J H, et al.. Integrated real-time optofluidic SERS via a liquid-core/liquid-cladding waveguide[J]. RSC Advances, 2015, 5(2):922-927. doi: 10.1039/C4RA11027G [67] YAZDI S H, WHITE I M. Optofluidic surface enhanced Raman spectroscopy microsystem forsensitive and repeatable on-site detection of chemical contaminants[J]. Analytical Chemistry, 2012, 84(18):7992-7998. doi: 10.1021/ac301747b [68] HAN Z, LIU H, MENG J, et al.. Portable kit for identification and detection of drugs in human urine using surface-enhanced Raman spectroscopy[J]. Analytical Chemistry, 2015, 87(18):9500-9506. doi: 10.1021/acs.analchem.5b02899 [69] KIM A, BARCELO S J, WILLIAMS R S, et al.. Melamine sensing in milk products by using surface enhanced Raman scattering[J]. Analytical Chemistry, 2012, 84(21):9303-9309. doi: 10.1021/ac302025q [70] VILLA J E L, POPPI R J. Aportable SERS method for the determination of uric acid using a paper-based substrate and multivariate curve resolution[J]. Analyst, 2016, 141(6):1966-1972. doi: 10.1039/C5AN02398J -





 下载:
下载: